1. ņä£ ļĪĀ
ņĀäļĀźļ░śļÅäņ▓┤(Power semiconductor)ļŖö ņĀäļĀźņÜ® Ēīīņøī ņŖżņ£äņ╣Ł ņåīņ×É(Power switching device)ņÖĆ ņĀ£ņ¢┤ ICļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņĀäņ×ÉĻĖ░ĻĖ░ņŚÉ ņŻ╝ņ×ģļÉśļŖö ņĀäļĀźņØä ļ│ĆĒÖś ļ░Å ļČäļ░░, Ļ┤Ćļ”¼ĒĢśļŖö ņŚŁĒĢĀņØä ĒĢśļŖö ļ░śļÅäņ▓┤ļĪ£, ņØ╝ļ░ś ļ░śļÅäņ▓┤ņŚÉ ļ╣äĒĢ┤ Ļ│Ā ņŗĀļó░ņä▒ņØ┤ ņÜöĻĄ¼ļÉśļ®░, ĒĢśņØ┤ļĖīļ”¼ļō£ ņ×ÉļÅÖņ░©, ņĀäĻĖ░ ņ×ÉļÅÖņ░© ļō▒ņØś Ļ░£ļ░£ļĪ£ ĻĘĖ ņłśņÜöĻ░Ć ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŗż. ņĀäļĀźļ░śļÅäņ▓┤ ļ¬©ļōłņØĆ ņĀäļĀźļ░śļÅäņ▓┤ ņåīņ×É ļ░Å Ēī©Ēéżņ¦Ģ ņåīņ×¼ņØś ļ¬©ļōł ņ¦æņĀüĒÖö ņäżĻ│ä ĻĖ░ņłĀ, ņĀ£ņĪ░ Ļ│ĄņĀĢĻĖ░ņłĀ, ĒŖ╣ņä▒ņŗ£ĒŚś ļ░Å ņŗĀļó░ņä▒ ĒÅēĻ░Ć ļō▒ņØś ņŻ╝ņÜö ĻĖ░ņłĀņØä ĒåĄĒĢ┤ ĻĄ¼ĒśäļÉśļŖö Ļ▓āņ£╝ļĪ£, ĒŖ╣Ē׳ ņ╣£ĒÖśĻ▓Į ņ×ÉļÅÖņ░©ņØĖ ĒĢśņØ┤ļĖīļ”¼ļō£ ņ×ÉļÅÖņ░© ļ░Å ņĀäĻĖ░ņ×ÉļÅÖņ░©ņŚÉ ņĀüņÜ®ļÉśļŖö ņĀäļĀźļ¬©ļōłņØĆ Ļ│Āņś© ļ░Å ņ¦äļÅÖ ļō▒ņØś ņŚ┤ņĢģĒĢ£ ĒÖśĻ▓ĮņŚÉņä£ ļÅÖņ×æļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ļåÆņØĆ ņŗĀļó░ņä▒ņØ┤ ņÜöĻĄ¼ļÉ£ļŗż
1,2). ņĀäļĀźļ░śļÅäņ▓┤ņÜ® ņåöļŹöļĪ£ Sn-PbĻ│ä ņåöļŹöĻ░Ć ņŻ╝ļĪ£ ņé¼ņÜ®ļÉśņŚłņ£╝ļéś, ņ╣£ĒÖśĻ▓Į ĻĘ£ņĀ£ņØĖ ņ×ÉļÅÖņ░© ĒÅÉņ░©ņ▓śļ”¼ņ¦Ćņ╣©(ELV, End of Life Vehicle) ļ▓ĢĻĘ£ļĪ£ ņØĖĒĢ┤ ņ×ÉļÅÖņ░©ņÜ® ņĀäļĀź ļ░śļÅäņ▓┤ņŚÉ ļīĆĒĢ£ ļ¼┤ņŚ░ņåöļŹö ņĀüņÜ®ņØ┤ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż
3,4). ņØ┤ļź╝ ļīĆņ▓┤ĒĢĀ ņåöļŹö Ēøäļ│┤ļĪ£ ļ╣äĻĄÉņĀü ņĀ¢ņØīņä▒ ļ░Å Ēü¼ļ”Į ĒŖ╣ņä▒ņØ┤ ņÜ░ņłśĒĢ£ Sn-SbĻ│ä ņåöļŹöĻ░Ć Ļ▒░ļĪĀļÉśĻ│Ā ņ׳ņ£╝ļ®░, Ļ│Āņś©, Ļ│ĀņŖĄ ļ░Å ņ¦äļÅÖ ļō▒ņØś ņé¼ņÜ® ĒÖśĻ▓ĮņŚÉ ļö░ļźĖ ņŗĀļó░ņä▒ ņŚ░ĻĄ¼Ļ░Ć ņ¦äĒ¢ē ļÉśĻ│Ā ņ׳ļŗż
5,6). ĒĢśņ¦Ćļ¦ī ņåöļŹöļ¦ü Ļ│ĄņĀĢ ņżæ ņé¼ņÜ®ļÉśļŖö Ēöīļ¤ŁņŖżļéś ņäĖņ▓ÖĻ│ĄņĀĢ ļśÉļŖö ļīĆĻĖ░ ņżæņØś ņŚ╝ļČä, ņŖĄĻĖ░ ļō▒ņØś ņé¼ņÜ®ĒÖśĻ▓ĮņŚÉ ļīĆĒĢ£ ņåöļŹö ņĀæĒĢ®ļČĆņØś ļČĆņŗØ ņŗĀļó░ņä▒ņŚÉ Ļ┤ĆĒĢ£ ņŚ░ĻĄ¼ļŖö ļ»Ėļ╣äĒĢ£ ņŗżņĀĢņØ┤ļŗż
7). ļé┤ņŗØņä▒ņØä ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ£ ņØ╝ļ░śņĀüņØĖ ļČĆņŗØ ņŗ£ĒŚśļ░®ļ▓Ģņ£╝ļĪ£ļŖö ņŚ╝ņłśļČäļ¼┤ņŗ£ĒŚśļ▓Ģ(Salt Spray Test)Ļ│╝ CASS(Copper Accelerated Acetic Acid Salt Spray)ņŗ£ĒŚś, ņĀäĻĖ░ĒÖöĒĢÖņĀü ļČäĻĘ╣ņŗ£ĒŚśļ░®ļ▓ĢņØ┤ ņ׳ļŗż. ĒĢśņ¦Ćļ¦ī ļČĆņŗØ ļ®┤ņĀüļźĀņŚÉ ņØśĒĢ£ Rating NumberļĪ£ ņåöļŹöņØś ļé┤ņŗØņä▒ņØä ĒÅēĻ░ĆļŖö ņŚ╝ņłśļČäļ¼┤ņŗ£ĒŚśļ▓Ģ ļ░Å CASS ņŗ£ĒŚśļ▓ĢņØĆ ņŗ£ĒŚś Ļ▓Ćņé¼ņ×ÉņØś ņŻ╝Ļ┤ĆņØ┤ Ļ░£ņ×ģļÉĀ ņŚ¼ņ¦ĆĻ░Ć ļ¦ÄņĢä, ņŗ£ĒŚśĻ▓░Ļ│╝ņŚÉ ļīĆĒĢ£ Ļ░ØĻ┤ĆņĀüņØĖ ņĀĢļ¤ēĒÖöĻ░Ć ņēĮņ¦Ć ņĢŖļŗżļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż
8,9).
ņØ┤ņŚÉ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö, ļŗ©ĻĖ░Ļ░äņŚÉ ņåöļŹöņØś ļé┤ņŗØņä▒ņØä ņĀĢļ¤ēņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŗżļŖö ņןņĀÉņØä Ļ░Ćņ¦ä ņĀäĻĖ░ĒÖöĒĢÖņĀü ļČĆņŗØņŗ£ĒŚś ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢśņŚ¼ Sb ĒĢ©ļ¤ēņŚÉ ļö░ļźĖ Sn-xSbĻ│ä ņåöļŹöņØś ļČĆņŗØĒŖ╣ņä▒ņØä ļ╣äĻĄÉ ĒÅēĻ░ĆĒĢśņśĆļŗż. ņØ┤ļź╝ ĻĖ░ņ┤łļĪ£ Sn-xSbĻ│ä ņåöļŹöņØś ņĀäĻĖ░ĒÖöĒĢÖņĀü ļČĆņŗØĒŖ╣ņä▒ņØä ĒåĄĒĢ┤ ņĀäļĀźļ░śļÅäņ▓┤ņÜ® Ļ│Āņś© ņåöļŹöņØś ņĀüĒĢ®ņŚ¼ļČĆļź╝ ļ╣äĻĄÉ, ĒÅēĻ░ĆĒĢśņśĆļŗż.
2. ņŗżĒŚśļ░®ļ▓Ģ
2.1 ņŗ£ĒŚś ņŗ£ĒÄĖ ņĀ£ņ×æ
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö Sb ĒĢ©ļ¤ēņŚÉ ļö░ļźĖ ņåöļŹöņØś ņĀäĻĖ░ĒÖöĒĢÖņĀü ĒŖ╣ņä▒ņØä ļČäņäØĒĢśĻ│Āņ×É Sn-5Sb, Sn-8Sb, Sn-10Sb, Sn- 8Sb-3Ag ņĪ░ņä▒ņØś ņåöļŹöļź╝ ņé¼ņÜ®ĒĢśņśĆļŗż. Ļ░üĻ░üņØś ņåöļŹöļź╝ ņŚÉĒÅŁņŗ£ ņłśņ¦ĆļĪ£ ļ¦łņÜ┤Ēīģ Ēøä, ņŚ░ļ¦łņ¦ĆņÖĆ ņĢīļŻ©ļ»Ėļéś ĒīīņÜ░ļŹöļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ĻĖ░Ļ│äņĀü ņŚ░ļ¦łļź╝ ņŗżņŗ£ĒĢśņśĆļŗż. ĻĘĖ Ēøä, ņåöļŹöļź╝ 0.5cm
#1 ļ®┤ņĀüļ¦ī ļģĖņČ£ļÉśĻ▓ī ņŗ£ĒÄĖņØä ņĀ£ņ×æĒĢśņśĆļŗż. ņŗ£ĒŚś ņŗ£ĒÄĖņØś ņĀ£ņ×æ ļ¬©ņŗØļÅäļź╝
Fig. 1 ņŚÉ ļéśĒāĆļé┤ņŚłļŗż.
Fig.┬Ā1
Schematic of fabricated of test sample

2.2 ļ»ĖņäĖĻĄ¼ņĪ░ ļČäņäØ
Sb ĒĢ©ļ¤ēņŚÉ ļö░ļźĖ Sn-xSbĻ│ä ņåöļŹöņØś ļ»ĖņäĖĻĄ¼ņĪ░ ļ░Å ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ĒśĢņāüņØä Ļ┤Ćņ░░ĒĢśĻĖ░ ņ£äĒĢ┤ EPMA(Electron Probe Micro Analyzer)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ Ļ┤Ćņ░░ĒĢśņśĆņ£╝ļ®░, XRD(X-ray diffraction)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ĒśĢņä▒ļÉ£ ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ņóģļźśļź╝ ļČäņäØĒĢśņśĆļŗż.
2.3 ļČäĻĘ╣ ņŗ£ĒŚś
SbĒĢ©ļ¤ēņŚÉ ļö░ļźĖ ļČĆņŗØ ĒŖ╣ņä▒ņØä ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ HOKUTO DENKO ńżŠņØś HZ-7000 ļ¬©ļŹĖņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, 25 ┬░C, 3.5 wt. % 1 mole ļåŹļÅäņØś NaCl ņÜ®ņĢĪņŚÉņä£ ņĀäĻĖ░ĒÖöĒĢÖņĀü ļČäĻĘ╣ ņŗ£ĒŚśņØä ņ¦äĒ¢ēĒĢśņśĆļŗż. ņĖĪņĀĢņŚÉ ņé¼ņÜ®ļÉ£ Ēæ£ņżĆņĀäĻĘ╣ņ£╝ļĪ£ ņØĆ/ņŚ╝ĒÖöņØĆ(Ag/AgCl) ņĀäĻĘ╣ņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, ļČäĻĘ╣ ĒŖ╣ņä▒ņØĆ -1200 mVņŚÉņä£ +600 mV ļ▓öņ£äņØś ņĀäņ£äņŚÉņä£ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ņŗ£ĒŚśņŗ£ĒÄĖņŚÉ ņĀäņ£äļź╝ ņØĖĻ░ĆĒĢ£ Ēøä, ļ░£ņāØļÉśļŖö ņĀäļźśņØś ņØ╝ļ░śņĀüņØĖ ļČäĻĘ╣ Ļ│ĪņäĀ ĻĘĖļלĒöäļź╝
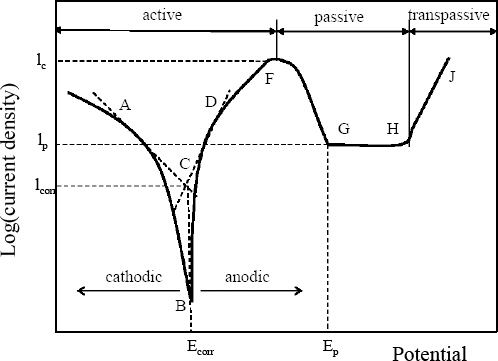
Fig. 2ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. AB ļ░Å BFļŖö Ļ░üĻ░ü ņØīĻĘ╣ ļ░Å ņ¢æĻĘ╣ ļČäĻĘ╣ Ļ│ĪņäĀņØä ļéśĒāĆļéĖļŗż. ĒāĆĒÄĀ ņÖĖņéĮļ▓Ģ(Tafel extrapolation)ņØä ņé¼ņÜ®ĒĢśņŚ¼ ņ¢æĻĘ╣ ļ░Å ņØīĻĘ╣ ļČäĻĘ╣ Ļ│ĪņäĀņŚÉ ņĀæņäĀņØä ĻĄ¼ĒĢśņśĆļŗż. ļæÉ ņĀæņäĀņØś ĻĄÉņĀÉ(C)ņØä ļČĆņŗØņĀäļźśļ░ĆļÅä(I
corr)ļØ╝ ĒĢśļ®░, ņØ┤ļĢīņØś ņĀäņ£ä Ļ░ÆņØä ļČĆņŗØņĀäņ£ä(E
corr)ļØ╝Ļ│Ā ĒĢ£ļŗż. ņĀäļźśļ░ĆļÅäĻ░Ć ņĄ£ļīĆĻ░Ć ļÉśļŖö ņ¦ĆņĀÉ(F)ņØś ņĀäņ£äļź╝ ļČĆļÅÖĒā£ĒÖö ņĀäņ£ä(E
p), ņĀäļźśļź╝ ļČĆļÅÖĒā£ĒÖö ņ×äĻ│äņĀäļźś(I
c)ļØ╝ ĒĢ£ļŗż. FGņśüņŚŁņŚÉņä£ ļ│ĄĒĢ® ņé░ĒÖöļ¼╝ņØś ņāØņä▒ņ£╝ļĪ£ ļČĆņŗØ ņĀäļźśļ░ĆļÅäĻ░Ć Ļ░ÉņåīļÉśļ®░, ņĀÉ HļŖö ļČĆļÅÖĒā£ņśüņŚŁ ņĀäļźśļ░ĆļÅä(I
p)ļØ╝Ļ│Ā ĒĢ£ļŗż. ĻĘĖ Ēøä, ņé░ĒÖöļ¼╝ņØś ĒīīĻ┤┤Ļ░Ć ņŗ£ņ×æļÉĀ ļĢīĻ╣īņ¦Ć ļ╣äĻĄÉņĀü ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉ£ļŗż. ņØ┤ļź╝ ĻĖ░ļ░śņ£╝ļĪ£ Sn- xSbĻ│ä ņåöļŹöņØś E
corr, I
corr, E
p, I
c ļ░Å R
p Ļ░ÆņØä ņĖĪņĀĢĒĢśņśĆļŗż
10).
Fig.┬Ā2
Schematic polarization curve of passivable metals
3. Ļ▓░Ļ│╝ ļ░Å Ļ│Āņ░░
3.1 ļ»ĖņäĖĻĄ¼ņĪ░ Ļ┤Ćņ░░
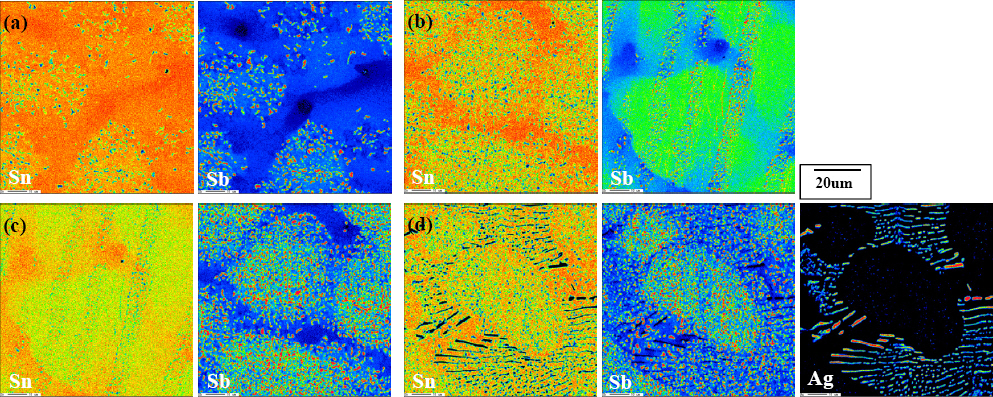
Sn-xSb ņåöļŹöņØś Sb ĒĢ©ļ¤ēņŚÉ ļö░ļźĖ ļ»ĖņäĖĻĄ¼ņĪ░ļź╝ Ļ┤Ćņ░░ĒĢ£ EPMA mapping ņØ┤ļ»Ėņ¦Ćļź╝
Fig. 3ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. (a), (b), (c) ņŚÉņä£ļŖö ╬▓-Sn ņĪ░ņ¦ü ļé┤ņŚÉ ņłś um ņØ┤ĒĢśņØś SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ļ»ĖņäĖĒĢśĻ▓ī ļČäņé░ļÉśņ¢┤ ņ׳ņ£╝ļ®░, (d) ļŖö ╬▓-Sn ņĪ░ņ¦ü ļé┤ņŚÉ SnSb, Ag
3Sn ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ļČäņé░ļÉśņ¢┤ ņ׳ļŗż.
Fig.┬Ā3
EPMA mapping images of various solders:(a) Sn-5Sb (b) Sn-8Sb (c) Sn-10Sb (d) Sn-8Sb-3Ag
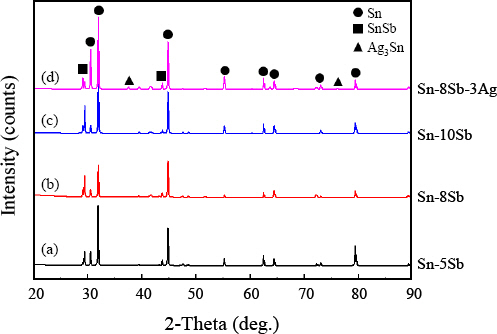
Sb ĒĢ©ļ¤ēņŚÉ ļö░ļźĖ ņäØņČ£ņāü ļ░Å ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś XRD ļČäņäØ Ļ▓░Ļ│╝ļź╝
Fig. 4ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. Sn-(5, 8, 10)Sb ņåöļŹöņØś Ļ▓ĮņÜ░ Sn, SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ Ļ▓ĆņČ£ ļÉśņŚłņ£╝ļ®░, SnSb ĒÖöĒĢ®ļ¼╝ņØś Ļ▓ĮņÜ░ SbņØś ĒĢ©ļ¤ēņØ┤ ļåÆņĢäņ¦łņłśļĪØ SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ņ”ØĻ░ĆĒĢśņśĆļŗż. Sn-8Sb-3Ag ņåöļŹöļŖö Sn, SnSb ņÖĖņŚÉ Ag
3Sn ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ Ļ▓ĆņČ£ļÉśņŚłļŗż.
Fig.┬Ā4
XRD patterns of various solders:(a) Sn-5Sb (b) Sn-8Sb (c) Sn-10Sb (d) Sn-8Sb-3Ag
3.2 ļČäĻĘ╣ ĒŖ╣ņä▒ ļ╣äĻĄÉ
-1200 mV ~ +600 mV ņĀäņ£ä ņé¼ņØ┤ņŚÉņä£ ņĖĪņĀĢļÉ£ Sn- xSb ņåöļŹöņØś ņØīĻĘ╣ ļ░Å ņ¢æĻĘ╣ ļČäĻĘ╣ Ļ│ĪņäĀņØä
Fig. 5ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņØ┤ļĢīņØś ļČäĻĘ╣ Ļ│ĪņäĀ Ļ▓░Ļ│╝ļź╝ ĒåĄĒĢśņŚ¼ ņĖĪņĀĢļÉ£ ╬▓
a, ╬▓
b, E
corr, I
corr, E
p, I
c Ļ░ÆņØä
Table 1 ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. E
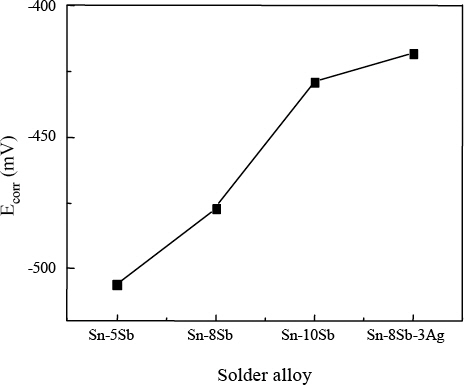
corrņØś Ļ▓ĮņÜ░ Sn-5SbļŖö -506mV, Sn-8SbļŖö -477mV, Sn- 10SbļŖö -429mV, Sn-8Sb-3AgļŖö -418mVļĪ£ ņĖĪņĀĢļÉśņŚłņ£╝ļ®░, ņåöļŹö ņĪ░ņä▒ņŚÉ ļö░ļźĖ E
corr ĻĘĖļלĒöäļź╝
Fig. 6 ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. SbņØś ĒĢ©ļ¤ēņØ┤ ņ”ØĻ░ĆĒĢĀņłśļĪØ E
corrņØ┤ ļåÆĻ▓ī ņĖĪņĀĢļÉśļŖö ņØ┤ņ£ĀļŖö Sn-xSbĻ│ä ņåöļŹöņŚÉ ņĪ┤ņ×¼ĒĢśļŖö SnņØ┤ Ļ░Ćņן ļ©╝ņĀĆ ļČĆņŗØņØ┤ ņ¦äĒ¢ēļÉśĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż. ņØ┤ļŖö Ēæ£ņżĆ ņĀäĻĘ╣ ņĀäņ£äņŚÉ ļö░ļØ╝ Sb, Ag ļ│┤ļŗż Sn Ļ░ÆņØ┤ ņāüļīĆņĀüņ£╝ļĪ£ ļé«ņĢä SnņØś ĒĢ©ļ¤ēņØ┤ ļåÆņØĆ Sn-5Sb ņåöļŹöņØś E
corrņØ┤ Ļ░Ćņן ļé«Ļ▓ī ņĖĪņĀĢļÉśņŚłļŗż. Ēæ£ņżĆ ņĀäĻĘ╣ ņĀäņ£äļź╝
Table 2ņŚÉ ļéśĒāĆļé┤ņŚłļŗż
11).
Fig┬Ā5
Polarization curves of Sn-xSb solder alloys in 3.5 wt.% NaCl solution

Fig.┬Ā6
Ecorr value during polarization of the Sn-xSb solder alloys in 3.5%NaCl solution
Table┬Ā1
Experimental data of the Sn-xSb solders alloys under polarization in 3.5 %NaCl solution
|
Solder |
╬▓a (mV/dec) |
╬▓c (mV/dec) |
Ecorr (mV) |
Icorr (uA/cm2) |
Rp (Ōä”┬Ęcm2) |
Ep (mV) |
Ic (A/cm2) |
|
Sn-5Sb |
106.99 |
130.41 |
-506 |
5.01 |
5.10├Ś103 |
34.31 |
0.0214 |
|
Sn-8Sb |
83.62 |
121.18 |
-477 |
7.74 |
2.79├Ś103 |
-12.16 |
0.018 |
|
Sn-10Sb |
31.22 |
26.66 |
-429 |
7.96 |
2.32├Ś103 |
-71.15 |
1.48 |
|
Sn-8Sb-3Ag |
35.68 |
133.23 |
-418 |
9.19 |
1.33├Ś103 |
-1.16 |
0.017 |
Table┬Ā2
Standard electrode potentials of Sn, Sb, and Ag
|
Electrode reaction |
Standard potential at 25┬░C (V vs SHE) |
|
Sn2++2e- ŌåÆ Sn |
-0.136 |
|
Sb3++3e- ŌåÆ Sb |
0.10 |
|
Ag++e- ŌåÆ Ag |
0.799 |
ĻĖ░ņĪ┤ ļ¼ĖĒŚīņŚÉ ļö░ļź┤ļ®┤ ņäĀĒśĢļČäĻĘ╣ņĀĆĒĢŁ(R
p)ņØĆ ņĀäĻĘ╣Ēæ£ļ®┤ņŚÉņä£ņØś ļČĆņŗØņåŹļÅäņÖĆ ļ░śļ╣äļĪĆņĀü Ļ┤ĆĻ│äĻ░Ć ņ׳ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļ®░, Stern-Geary ņŗØņØä ņé¼ņÜ®ĒĢśņŚ¼ R
pļź╝ ĻĄ¼ĒĢśņśĆļŗż
12,13). ņØ┤ļĢīņØś ╬▓
a ņÖĆ ╬▓
c ļŖö ņ¢æĻĘ╣ ļ░Å ņØīĻĘ╣ņØś ĒāĆĒÄĀ ĻĖ░ņÜĖĻĖ░ņØ┤ļ®░, ņåöļŹö ņĪ░ņä▒ņŚÉ ļö░ļØ╝ Ļ│äņé░ļÉ£ R
pļź╝
Fig. 7 ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. Sn-5SbļŖö 5.10├Ś10
3 Ōä”┬Ęcm
#1, Sn-8SbļŖö 2.79├Ś10
3 Ōä”┬Ęcm
#1, Sn-10SbļŖö 2.32├Ś10
3 Ōä”┬Ęcm
#1, Sn-8Sb-3AgļŖö 1.33├Ś10
3 Ōä”┬Ęcm
#1 ņØś Ļ░ÆņØä ĻĄ¼ĒĢśņśĆļŗż.
Fig.┬Ā7
Rp value during polarization of the Sn-xSb solder alloys in 3.5%NaCl solution

ĻĖ░ņĪ┤ ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤, ņåöļŹö ļé┤ļČĆņØś ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝Ļ│╝ Sn ņé¼ņØ┤ņØś ņĀäņ£äņ░©ņŚÉ ņØśĒĢ£ Ļ░łļ░öļŗē ļČĆņŗØņØś ĒÜ©Ļ│╝ļĪ£ ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ņ”ØĻ░ĆĒĢ©ņŚÉ ļö░ļØ╝ ļČĆņŗØņĀĆĒĢŁņØ┤ ļé«Ļ▓ī ņĖĪņĀĢļÉ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż
14,15). ļö░ļØ╝ņä£ Sb ĒĢ©ļ¤ēņØ┤ ņ”ØĻ░ĆĒĢ©ņŚÉ ļö░ļØ╝ SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ņ”ØĻ░ĆĒĢśĻ▓ī ļÉśņ¢┤ R
pĻ░Ć ļé«Ļ▓ī ņĖĪņĀĢļÉ£ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż
16). ļśÉĒĢ£, Sn-8Sb-3Ag ņåöļŹöņŚÉņä£ļŖö SnSb ļ░Å Ag
3Sn ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ņāØņä▒ņŚÉ ļö░ļźĖ R
pĻ░Ć ļé«Ļ▓ī ņĖĪņĀĢļÉ£ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.
4. Ļ▓░ ļĪĀ
SbĒĢ©ļ¤ēņŚÉ ļö░ļźĖ Sn-xSbĻ│ä ņåöļŹöņØś 25┬░C, 3.5 wt% NaCl ņÜ®ņĢĪņŚÉņä£ ļČĆņŗØ ņŗ£ĒŚśņØä ņ¦äĒ¢ēĒĢśņśĆļŗż. ņØ┤ļź╝ ĻĖ░ņ┤łļĪ£ Sn-xSbĻ│ä ņåöļŹöņØś ņĀäĻĖ░ĒÖöĒĢÖņĀü ļČĆņŗØĒŖ╣ņä▒ ļ░Å ņäĀĒśĢļČäĻĘ╣ņĀĆĒĢŁ(RP)ņØä ļ╣äĻĄÉĒĢśņśĆļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ▓░Ļ│╝ļź╝ ĒåĄĒĢ┤ ļŗżņØīĻ│╝ Ļ░ÖņØĆ Ļ▓░ļĪĀņØä ņ¢╗ņŚłļŗż.
1) Sn-xSbĻ│ä ņåöļŹöņØś ļ»ĖņäĖĻĄ¼ņĪ░ Ļ┤Ćņ░░Ļ▓░Ļ│╝, Sn-(5, 8, 10)Sb ņåöļŹöņØś Ļ▓ĮņÜ░ ╬▓-Sn ņĪ░ņ¦ü ļé┤ņŚÉ ņłś um ņØ┤ĒĢśņØś SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ļ»ĖņäĖĒĢśĻ▓ī ļČäņé░ļÉśņ¢┤ ņ׳ņ£╝ļ®░, SbņØś ĒĢ©ļ¤ēņØ┤ ļåÆņĢäņ¦łņłśļĪØ SnSb ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ņ¢æņØĆ ņ”ØĻ░ĆĒĢśņśĆļŗż. Sn-8Sb-3Ag ņåöļŹöņØś Ļ▓ĮņÜ░ ╬▓-Sn ņĪ░ņ¦ü ļé┤ņŚÉ SnSb, Ag3Sn ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØ┤ ļČäņé░ļÉśņŚłļŗż.
2) ļČĆņŗØņĀäņ£ä ļ╣äĻĄÉ Ļ▓░Ļ│╝, SbņØś ĒĢ©ļ¤ēņØ┤ ņ”ØĻ░ĆĒĢĀņłśļĪØ ļČĆņŗØņĀäņ£äĻ░Ć ļåÆĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż. SbņØś ĒĢ©ļ¤ēņØ┤ ņ”ØĻ░ĆĒĢĀņłśļĪØ ļČĆņŗØņĀäņ£äĻ░Ć ļåÆĻ▓ī ņĖĪņĀĢļÉśļŖö ņØ┤ņ£ĀļŖö Ēæ£ņżĆ ņĀäĻĘ╣ ņĀäņ£äņŚÉ ļö░ļØ╝ Sb, Ag ļ│┤ļŗż Sn Ļ░ÆņØ┤ ņāüļīĆņĀüņ£╝ļĪ£ ļé«ņĢä SnņØś ĒĢ©ļ¤ēņØ┤ ļåÆņØĆ Sn-5Sb ņåöļŹöņØś ļČĆņŗØņĀäņ£äĻ░Ć Ļ░Ćņן ļé«Ļ▓ī ņĖĪņĀĢļÉ£ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.
3) ņäĀĒśĢļČäĻĘ╣ņĀĆĒĢŁ ļ╣äĻĄÉ Ļ▓░Ļ│╝, SbņÖĆ AgņØś ĒĢ©ļ¤ēņØ┤ ņ”ØĻ░ĆĒĢĀņłśļĪØ, ņäĀĒśĢļČäĻĘ╣ņĀĆĒĢŁņØ┤ ļé«Ļ▓ī ņĖĪņĀĢļÉśņŚłļŗż. SnSb ļ░Å Ag3Sn ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ņ”ØĻ░ĆņŚÉ ļö░ļźĖ SnĻ│╝ ĻĖłņåŹĻ░äĒÖöĒĢ®ļ¼╝ņØś ņĀäņ£äņ░©ņŚÉ ņØśĒĢ£ Ļ░łļ░öļŗē ļČĆņŗØņØś ĒÜ©Ļ│╝ļĪ£ ļČĆņŗØņĀĆĒĢŁņØ┤ ļé«Ļ▓ī ņĖĪņĀĢļÉ£ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.
Acknowledgments
ļ│Ė ņŚ░ĻĄ¼ļŖö ņé░ņŚģĒåĄņāüņ×ÉņøÉļČĆ ĻĖĆļĪ£ļ▓īņĀäļ¼ĖĻĖ░ņłĀĻ░£ļ░£ņé¼ņŚģņØś ņ¦ĆņøÉņ£╝ļĪ£ ņłśĒ¢ēļÉśņŚłņŖĄļŗłļŗż.
References
3. J. Biela, M. Schweizer, S. Waffler, and W. Kolar. Johann, SiC versus Si-Evaluation of Potentials for Performance Im-provement of Inverter and DC-DC Converter Systems by SiC Power Semiconductors,
IEEE Transactions on Industrial Electronics. 58(7) (2011) 2872ŌĆō2882.
https://doi.org/10.1109/TIE.2010.2072896
[CROSSREF] 5. J. MCCABE. RODNEY and E. FINE. MORRIS, Creep of Tin, Sb Solution Strengthened Tin, and SbSn Precipitate-Strengthened Tin, Metallurgical and Materials Transactions. 33A (2002) 1531ŌĆō1539.
6. J. H. Son, M. K. Kim, D. Y. Yu, Y. H. Ko, J. W. Yoon, C. W. Lee, Y. B. Park, and J. H. Bang, Thermal Aging Characteris-tics of Sn-xSb Solder for Automotive Power Module,
Journal of Welding and Joining. 35(5) (2017) 38ŌĆō47.
https://doi.org/10.5781/JWJ.2017.35.5.6
[CROSSREF] [PDF] 7. W. S. Hong and K. B. Kim, Tafel Characteristics by Elec-trochemical Reaction of SnAgCu Pb-Free Solder,
Korea Journal of Materials Research. 15(8) (2005) 536ŌĆō542.
[CROSSREF] [PDF] 8. BO. LIU, TAE-KYU. LEE, and KUO-CHUAN. LIU, Impact of 5% NaCl Salt Spray Pretreatment on the Long-Term Reliability of Wafer-Level Packages with Sn-Pb and Sn-Ag-Cu Solder Interconnects,
Journal of ELECTRONIC MATERIALS. 40(10) (2011) 2111ŌĆō2118.
https://doi.org/10.1007/s11664-011-1705-y
[CROSSREF] 9. Hyuntaeck. Lim, Pilkyu. Kim, Hoemin. Jeong, and Sungho. Jeong, Enhancement of abrasion and corrosion resistance of duplex stainless steel by laser shock peening,
Journal of Materials Processing Technology. 212(6) (2012) 1347ŌĆō1354.
https://doi.org/10.1016/j.jmatprotec.2012.01.023
[CROSSREF] 11. Corrosion. 13 9th Ed. Metals Handbook (ASM) International; Metals Park, OH: (1987)
12. Tait. William Stephen, An introduction to electrochemical corrosion testing for practicing and engineers and scientists, 1ŌĆō55. (1904)
13. M. G. Fontana, Corrosion engineering, McGraw-Hill. 153-218 (1987)
15. Q. V. Bui, N. D. Nam, B. I. Noh, A. Kar, J. G. Kim, and S. B. Jung, Effect of Ag addition on the corrosion properties of Sn-based solder alloys,
Materials and Corrosion. 61(1) (2010) 30ŌĆō33.
https://doi.org/10.1002/maco.200905237
[CROSSREF] 16. Torres. Alberto, Hernandez. Luis, and Dominguez. Octavio, Effect of Antimony Additions on Corrosion and Mechanical Properties of Sn-Bi Eutectic Lead-Free Solder Alloy,
Materials Sciences and Applications. (2012) 355ŌĆō362.
https://doi.org/10.4236/msa.2012.36051
[CROSSREF]











 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print